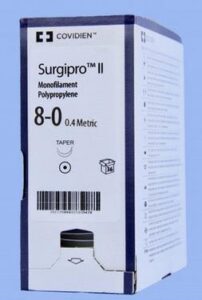
La Dirección Nacional de Vigilancia Sanitaria (DINAVISA), informa que, a través de la Dirección General de Vigilancia, tomó conocimiento acerca de la alerta emitida por el Instituto de Salud Pública – ISP (Chile) en la que informan el retiro de mercado del producto Surgipro™ II Sutura Polipropileno monofilamento 8-0 60 cm modelo VP-745-X de los lotes D1H2487Y y D1J2541Y; debido a que se han identificado errores de fabricación en el embalaje que pueden generar un orificio o arrugas en el sello de ventilación, lo que puede provocar una ruptura en la barrera estéril del producto.
El fabricante indica que entre los posibles daños de la ruptura en la barrera estéril se incluye la infección o en el caso de procedimientos oftálmicos en los que exista contacto directo con el paciente, la pérdida de visión. También señala que no hay recomendaciones adicionales para el tratamiento de aquellos pacientes en los que ya se han utilizado estas suturas no absorbibles. Estos pacientes deberán continuar con la monitorización de acuerdo a los protocolos de cuidados estándar de su centro médico.
Atendiendo que el producto cuenta con Registro Sanitario en el país, la DINAVISA se comunicó con el titular del registro sanitario y ya se encuentra realizando el retiro de mercado del producto; a su vez solicita a la población en general que en caso de que noten unidades de los lotes mencionados, no utilicen el producto y comuniquen al correo [email protected].
La Dirección Nacional de Vigilancia Sanitaria, a fin de salvaguardar la salud de la población, recomienda a los profesionales de la salud, pacientes y población en general:
– Adquirir productos que provengan de establecimientos autorizados.
– Si ha usado este dispositivo médico con las características antes citadas y presentó un evento adverso, puede notificarlo al correo [email protected]
ANTE LA DETECCIÓN DE CUALQUIER PRODUCTO SOSPECHOSO
NOTIFIQUE AL CORREO: [email protected]
Asunción, 29 de Mayo del 2023

![Logo de la [Institución Pública]](https://dinavisa.gov.py/wp-content/uploads/2023/08/cropped-cabecera-5.jpg)